ความร้อนมีปริมาณเท่าใด? การคำนวณปริมาณความร้อนระหว่างการถ่ายเทความร้อน ความจุความร้อนจำเพาะของสาร
« ฟิสิกส์ - ชั้นประถมศึกษาปีที่ 10"
การเปลี่ยนแปลงโดยรวมของสสารเกิดขึ้นในกระบวนการใด?
คุณจะเปลี่ยนสถานะการรวมตัวของสารได้อย่างไร?
คุณสามารถเปลี่ยนพลังงานภายในของร่างกายใดๆ ได้ด้วยการทำงาน ให้ความร้อน หรือในทางกลับกัน ทำให้เย็นลง
ดังนั้นเมื่อทำการตีโลหะงานจะเสร็จและให้ความร้อนขึ้นในขณะเดียวกันก็สามารถให้ความร้อนโลหะเหนือเปลวไฟที่กำลังลุกไหม้ได้
นอกจากนี้หากลูกสูบได้รับการแก้ไข (รูปที่ 13.5) ปริมาตรของก๊าซจะไม่เปลี่ยนแปลงเมื่อถูกความร้อนและไม่มีงานทำ แต่อุณหภูมิของแก๊สและดังนั้นมัน กำลังภายในกำลังเพิ่มขึ้น
พลังงานภายในสามารถเพิ่มหรือลดลงได้ ดังนั้นปริมาณความร้อนจึงสามารถเป็นบวกหรือลบได้
กระบวนการถ่ายโอนพลังงานจากร่างกายหนึ่งไปยังอีกร่างกายหนึ่งโดยไม่ต้องทำงานเรียกว่า การแลกเปลี่ยนความร้อน.
เรียกว่าการวัดเชิงปริมาณของการเปลี่ยนแปลงพลังงานภายในระหว่างการถ่ายเทความร้อน ปริมาณความร้อน.
ภาพโมเลกุลของการถ่ายเทความร้อน
ในระหว่างการแลกเปลี่ยนความร้อนที่ขอบเขตระหว่างวัตถุ ปฏิกิริยาระหว่างโมเลกุลที่เคลื่อนที่ช้าๆ ของวัตถุเย็นกับโมเลกุลที่เคลื่อนที่เร็วของวัตถุที่ร้อนจะเกิดขึ้น เป็นผลให้พลังงานจลน์ของโมเลกุลเท่ากัน และความเร็วของโมเลกุลของวัตถุเย็นเพิ่มขึ้น และความเร็วของวัตถุที่ร้อนลดลง
ในระหว่างการแลกเปลี่ยนความร้อน พลังงานจะไม่ถูกแปลงจากรูปแบบหนึ่งไปอีกรูปแบบหนึ่ง พลังงานภายในส่วนหนึ่งของวัตถุที่มีความร้อนมากกว่าจะถูกถ่ายโอนไปยังวัตถุที่มีความร้อนน้อยกว่า
ปริมาณความร้อนและความจุความร้อน
คุณรู้อยู่แล้วว่าเพื่อให้ความร้อนแก่มวล m จากอุณหภูมิ t 1 ถึงอุณหภูมิ t 2 จำเป็นต้องถ่ายโอนความร้อนจำนวนหนึ่งไป:
Q = ซม.(t 2 - เสื้อ 1) = ซม. Δt (13.5)
เมื่อร่างกายเย็นลง อุณหภูมิสุดท้ายของร่างกาย t 2 จะน้อยกว่าอุณหภูมิเริ่มต้น t 1 และปริมาณความร้อนที่ร่างกายปล่อยออกมาจะเป็นลบ
เรียกว่าสัมประสิทธิ์ c ในสูตร (13.5) ความจุความร้อนจำเพาะสาร
ความร้อนจำเพาะ- นี่คือปริมาณเป็นตัวเลขเท่ากับปริมาณความร้อนที่สารน้ำหนัก 1 กิโลกรัมได้รับหรือปล่อยออกมาเมื่ออุณหภูมิเปลี่ยนแปลง 1 เคลวิน
ความจุความร้อนจำเพาะของก๊าซขึ้นอยู่กับกระบวนการที่เกิดการถ่ายเทความร้อน หากคุณให้ความร้อนแก่แก๊สที่ความดันคงที่ ก๊าซจะขยายตัวและทำงานได้ ในการทำความร้อนก๊าซขึ้น 1 °C ที่ความดันคงที่ จะต้องถ่ายเทความร้อนมากกว่าการให้ความร้อนที่ปริมาตรคงที่ ซึ่งก๊าซจะมีความร้อนเพิ่มขึ้นเท่านั้น
ของเหลวและของแข็งจะขยายตัวเล็กน้อยเมื่อถูกความร้อน ความจุความร้อนจำเพาะที่ปริมาตรคงที่และความดันคงที่แตกต่างกันเล็กน้อย
ความร้อนจำเพาะการกลายเป็นไอ
ในการเปลี่ยนของเหลวให้เป็นไอน้ำในระหว่างกระบวนการเดือด จะต้องถ่ายเทความร้อนจำนวนหนึ่งไป อุณหภูมิของของเหลวไม่เปลี่ยนแปลงเมื่อเดือด การเปลี่ยนของเหลวเป็นไอที่อุณหภูมิคงที่ไม่ได้นำไปสู่การเพิ่มขึ้นของพลังงานจลน์ของโมเลกุล แต่จะมาพร้อมกับการเพิ่มขึ้นของพลังงานศักย์ของปฏิสัมพันธ์ของพวกมัน ท้ายที่สุดแล้ว ระยะห่างเฉลี่ยระหว่างโมเลกุลของก๊าซนั้นมากกว่าระหว่างโมเลกุลของเหลวมาก
ปริมาณที่เป็นตัวเลขเท่ากับปริมาณความร้อนที่ต้องใช้ในการแปลงของเหลวที่มีน้ำหนัก 1 กิโลกรัมเป็นไอน้ำที่อุณหภูมิคงที่เรียกว่า ความร้อนจำเพาะของการกลายเป็นไอ.
กระบวนการระเหยของของเหลวเกิดขึ้นที่อุณหภูมิใดก็ได้ ในขณะที่โมเลกุลที่เร็วที่สุดจะออกจากของเหลว และจะเย็นตัวลงในระหว่างการระเหย ความร้อนจำเพาะของการระเหยมีค่าเท่ากับความร้อนจำเพาะของการระเหย
ค่านี้แสดงด้วยตัวอักษร r และแสดงเป็นจูลต่อกิโลกรัม (J/kg)
ความร้อนจำเพาะของการกลายเป็นไอของน้ำมีค่าสูงมาก: r H20 = 2.256 · 10 6 J/kg ที่อุณหภูมิ 100 °C สำหรับของเหลวอื่นๆ เช่น แอลกอฮอล์ อีเทอร์ ปรอท น้ำมันก๊าด ความร้อนจำเพาะของการกลายเป็นไอจะน้อยกว่าน้ำ 3-10 เท่า
ในการแปลงของเหลวที่มีมวล m เป็นไอ จำเป็นต้องใช้ปริมาณความร้อนเท่ากับ:
คิว พี = RM (13.6)
เมื่อไอน้ำควบแน่น ความร้อนจะถูกปล่อยออกมาในปริมาณเท่ากัน:
ถาม k = -rm (13.7)
ความร้อนจำเพาะของฟิวชัน
เมื่อวัตถุที่เป็นผลึกละลาย ความร้อนทั้งหมดที่จ่ายไปจะไปเพิ่มพลังงานศักย์ของการมีปฏิสัมพันธ์ระหว่างโมเลกุล พลังงานจลน์ของโมเลกุลไม่เปลี่ยนแปลงเนื่องจากการหลอมละลายเกิดขึ้นที่อุณหภูมิคงที่
ค่าตัวเลขเท่ากับปริมาณความร้อนที่ต้องใช้ในการเปลี่ยนสารผลึกที่มีน้ำหนัก 1 กิโลกรัมที่จุดหลอมเหลวให้เป็นของเหลวเรียกว่า ความร้อนจำเพาะของฟิวชันและเขียนแทนด้วยตัวอักษร แล
เมื่อสารที่มีน้ำหนัก 1 กิโลกรัมตกผลึก ปริมาณความร้อนจะถูกปล่อยออกมาเท่ากันทุกประการกับที่ถูกดูดซับในระหว่างการหลอมละลาย
ความร้อนจำเพาะของการละลายน้ำแข็งค่อนข้างสูง: 3.34 10 5 J/kg
“ถ้าน้ำแข็งไม่มีความร้อนฟิวชันสูง ในฤดูใบไม้ผลิ มวลน้ำแข็งทั้งหมดจะต้องละลายในเวลาไม่กี่นาทีหรือวินาที เนื่องจากความร้อนจากอากาศถูกถ่ายเทไปยังน้ำแข็งอย่างต่อเนื่อง ผลที่ตามมาของสิ่งนี้จะเลวร้ายมาก ท้ายที่สุดแล้ว แม้ในสถานการณ์ปัจจุบัน น้ำท่วมใหญ่และกระแสน้ำที่รุนแรงก็เกิดขึ้นเมื่อน้ำแข็งหรือหิมะจำนวนมากละลาย” อาร์. แบล็ค ศตวรรษที่ 18
ในการละลายวัตถุที่เป็นผลึกที่มีมวล m จำเป็นต้องใช้ปริมาณความร้อนเท่ากับ:
คิวพีแอล = แลม. (13.8)
ปริมาณความร้อนที่ปล่อยออกมาระหว่างการตกผลึกของวัตถุมีค่าเท่ากับ:
Q cr = -แลม (13.9)
สมการสมดุลความร้อน
ให้เราพิจารณาการแลกเปลี่ยนความร้อนภายในระบบที่ประกอบด้วยวัตถุหลายตัวที่เริ่มแรกมี อุณหภูมิที่แตกต่างกันตัวอย่างเช่น การแลกเปลี่ยนความร้อนระหว่างน้ำในภาชนะกับลูกเหล็กร้อนที่ตกลงไปในน้ำ ตามกฎการอนุรักษ์พลังงาน ปริมาณความร้อนที่ปล่อยออกมาจากวัตถุหนึ่งจะมีค่าเท่ากับปริมาณความร้อนที่อีกวัตถุหนึ่งได้รับ
ปริมาณความร้อนที่ได้รับถือเป็นลบ ปริมาณความร้อนที่ได้รับถือว่าเป็นบวก ดังนั้น ปริมาณความร้อนรวม Q1 + Q2 = 0
หากการแลกเปลี่ยนความร้อนเกิดขึ้นระหว่างวัตถุหลายตัวในระบบแยก
ค 1 + ค 2 + ค 3 + ... = 0 (13.10)
เรียกว่าสมการ (13.10) สมการสมดุลความร้อน.
ในที่นี้ Q 1 Q 2, Q 3 คือปริมาณความร้อนที่ได้รับหรือปล่อยออกมาจากร่างกาย ปริมาณความร้อนเหล่านี้แสดงออกมาตามสูตร (13.5) หรือสูตร (13.6)-(13.9) หากการเปลี่ยนแปลงเฟสต่างๆ ของสาร (การหลอม การตกผลึก การกลายเป็นไอ การควบแน่น) เกิดขึ้นในระหว่างกระบวนการแลกเปลี่ยนความร้อน
ดังที่ทราบกันดีว่าในระหว่างกระบวนการทางกลต่างๆจะมีการเปลี่ยนแปลง พลังงานกล. การวัดการเปลี่ยนแปลงพลังงานกลคืองานของแรงที่ใช้กับระบบ:
ในระหว่างการแลกเปลี่ยนความร้อน พลังงานภายในร่างกายจะเกิดการเปลี่ยนแปลง การวัดการเปลี่ยนแปลงพลังงานภายในระหว่างการถ่ายเทความร้อนคือปริมาณความร้อน
ปริมาณความร้อนคือการวัดการเปลี่ยนแปลงพลังงานภายในที่ร่างกายได้รับ (หรือยอมแพ้) ระหว่างกระบวนการแลกเปลี่ยนความร้อน
ดังนั้นทั้งงานและปริมาณความร้อนจึงเป็นลักษณะการเปลี่ยนแปลงของพลังงาน แต่ไม่เหมือนกันกับพลังงาน พวกเขาไม่ได้ระบุลักษณะของระบบ แต่กำหนดกระบวนการเปลี่ยนพลังงานจากประเภทหนึ่งไปอีกประเภทหนึ่ง (จากร่างกายหนึ่งไปอีกร่างกายหนึ่ง) เมื่อสถานะเปลี่ยนแปลงและขึ้นอยู่กับลักษณะของกระบวนการอย่างมีนัยสำคัญ
ความแตกต่างที่สำคัญระหว่างงานกับปริมาณความร้อนก็คือ งานนั้นเป็นลักษณะของกระบวนการเปลี่ยนแปลงพลังงานภายในของระบบ ควบคู่ไปกับการเปลี่ยนแปลงพลังงานจากประเภทหนึ่งไปเป็นอีกประเภทหนึ่ง (จากกลไกไปเป็นภายใน) ปริมาณความร้อนเป็นลักษณะของกระบวนการถ่ายโอนพลังงานภายในจากร่างกายหนึ่งไปยังอีกร่างกายหนึ่ง (จากความร้อนมากขึ้นไปเป็นความร้อนน้อยลง) ซึ่งไม่ได้มาพร้อมกับการเปลี่ยนแปลงพลังงาน
ประสบการณ์แสดงให้เห็นว่าปริมาณความร้อนที่ต้องใช้ในการทำความร้อนร่างกายที่มีมวล m จากอุณหภูมิถึงอุณหภูมินั้นคำนวณโดยสูตร
ที่ไหนค - ความร้อนจำเพาะสาร;
![]()
หน่วย SI ของความจุความร้อนจำเพาะคือจูลต่อกิโลกรัมเคลวิน (J/(kg K))
ความร้อนจำเพาะ c เป็นตัวเลขเท่ากับปริมาณความร้อนที่ต้องส่งให้กับร่างกายที่มีน้ำหนัก 1 กิโลกรัมเพื่อให้ความร้อนขึ้น 1 เคลวิน
ความจุความร้อนร่างกายมีตัวเลขเท่ากับปริมาณความร้อนที่ต้องใช้ในการเปลี่ยนอุณหภูมิของร่างกาย 1 K:
![]()
หน่วย SI ของความจุความร้อนของร่างกายคือ จูลต่อเคลวิน (J/K)
ในการเปลี่ยนของเหลวให้เป็นไอน้ำที่อุณหภูมิคงที่จำเป็นต้องใช้ความร้อนจำนวนหนึ่ง
โดยที่ L คือความร้อนจำเพาะของการกลายเป็นไอ เมื่อไอน้ำควบแน่น ความร้อนจะถูกปล่อยออกมาในปริมาณเท่ากัน
ดังที่ทราบกันดีว่าในระหว่างกระบวนการทางกลต่างๆ การเปลี่ยนแปลงพลังงานกลจะเกิดขึ้น วอืม การวัดการเปลี่ยนแปลงพลังงานกลคืองานของแรงที่ใช้กับระบบ:
\(~\เดลต้า W_(meh) = A.\)
ในระหว่างการแลกเปลี่ยนความร้อน พลังงานภายในร่างกายจะเกิดการเปลี่ยนแปลง การวัดการเปลี่ยนแปลงพลังงานภายในระหว่างการถ่ายเทความร้อนคือปริมาณความร้อน
ปริมาณความร้อนคือการวัดการเปลี่ยนแปลงพลังงานภายในที่ร่างกายได้รับ (หรือยอมแพ้) ระหว่างกระบวนการแลกเปลี่ยนความร้อน
ดังนั้นทั้งงานและปริมาณความร้อนจึงเป็นลักษณะการเปลี่ยนแปลงของพลังงาน แต่ไม่เหมือนกันกับพลังงาน พวกเขาไม่ได้ระบุลักษณะของระบบ แต่กำหนดกระบวนการเปลี่ยนพลังงานจากประเภทหนึ่งไปอีกประเภทหนึ่ง (จากร่างกายหนึ่งไปอีกร่างกายหนึ่ง) เมื่อสถานะเปลี่ยนแปลงและขึ้นอยู่กับลักษณะของกระบวนการอย่างมีนัยสำคัญ
ความแตกต่างที่สำคัญระหว่างงานกับปริมาณความร้อนก็คือ งานนั้นเป็นลักษณะของกระบวนการเปลี่ยนแปลงพลังงานภายในของระบบ ควบคู่ไปกับการเปลี่ยนแปลงพลังงานจากประเภทหนึ่งไปเป็นอีกประเภทหนึ่ง (จากกลไกไปเป็นภายใน) ปริมาณความร้อนเป็นลักษณะของกระบวนการถ่ายโอนพลังงานภายในจากร่างกายหนึ่งไปยังอีกร่างกายหนึ่ง (จากความร้อนมากขึ้นไปเป็นความร้อนน้อยลง) ซึ่งไม่ได้มาพร้อมกับการเปลี่ยนแปลงพลังงาน
ประสบการณ์แสดงให้เห็นว่าปริมาณความร้อนที่ต้องใช้ในการทำความร้อนให้กับมวลกาย มเกี่ยวกับอุณหภูมิ ต 1 ถึงอุณหภูมิ ต 2 คำนวณโดยสูตร
\(~Q = ซม. (T_2 - T_1) = ซม. \เดลต้า T, \qquad (1)\)
ที่ไหน ค- ความจุความร้อนจำเพาะของสาร
\(~c = \frac(Q)(ม. (T_2 - T_1)).\)
หน่วย SI ของความจุความร้อนจำเพาะคือจูลต่อกิโลกรัมเคลวิน (J/(kg K))
ความร้อนจำเพาะ คเป็นตัวเลขเท่ากับปริมาณความร้อนที่ต้องให้ร่างกายหนัก 1 กิโลกรัม เพื่อให้ความร้อน 1 เคลวิน
ความจุความร้อนร่างกาย ค T เป็นตัวเลขเท่ากับปริมาณความร้อนที่ต้องใช้ในการเปลี่ยนอุณหภูมิของร่างกาย 1 K:
\(~C_T = \frac(Q)(T_2 - T_1) = ซม.\)
หน่วย SI ของความจุความร้อนของร่างกายคือ จูลต่อเคลวิน (J/K)
ในการเปลี่ยนของเหลวให้เป็นไอน้ำที่อุณหภูมิคงที่จำเป็นต้องใช้ความร้อนจำนวนหนึ่ง
\(~Q = Lm, \qquad (2)\)
ที่ไหน ล- ความร้อนจำเพาะของการกลายเป็นไอ เมื่อไอน้ำควบแน่น ความร้อนจะถูกปล่อยออกมาในปริมาณเท่ากัน
เพื่อที่จะหลอมละลายร่างกายที่เป็นผลึกชั่งน้ำหนัก มเมื่อถึงจุดหลอมเหลว ร่างกายจำเป็นต้องสื่อสารปริมาณความร้อน
\(~Q = \แลมบ์ดา m, \qquad (3)\)
ที่ไหน λ - ความร้อนจำเพาะของฟิวชัน เมื่อร่างกายตกผลึก ความร้อนจะถูกปล่อยออกมาในปริมาณเท่ากัน
ปริมาณความร้อนที่ปล่อยออกมาระหว่างการเผาไหม้เชื้อเพลิงโดยสมบูรณ์ ม,
\(~Q = คิวเอ็ม, \คิวควอด (4)\)
ที่ไหน ถาม- ความร้อนจำเพาะของการเผาไหม้
หน่วย SI ของความร้อนจำเพาะของการระเหย การหลอม และการเผาไหม้คือ จูลต่อกิโลกรัม (J/kg)
วรรณกรรม
Aksenovich L. A. ฟิสิกส์ มัธยม: ทฤษฎี. งาน การทดสอบ: หนังสือเรียน เบี้ยเลี้ยงสำหรับสถาบันการศึกษาทั่วไป สิ่งแวดล้อม การศึกษา / L. A. Aksenovich, N. N. Rakina, K. S. Farino; เอ็ด เค.เอส. ฟาริโน. - Mn.: Adukatsiya i vyhavanne, 2004. - หน้า 154-155.
การเปลี่ยนแปลงพลังงานภายในจากการทำงานมีลักษณะเฉพาะตามปริมาณงาน กล่าวคือ งานคือการวัดการเปลี่ยนแปลงพลังงานภายในในกระบวนการที่กำหนด การเปลี่ยนแปลงพลังงานภายในของร่างกายระหว่างการถ่ายเทความร้อนมีลักษณะเป็นปริมาณที่เรียกว่าปริมาณความร้อน
คือการเปลี่ยนแปลงพลังงานภายในร่างกายระหว่างกระบวนการถ่ายเทความร้อนโดยไม่ได้ทำงาน ปริมาณความร้อนจะระบุด้วยตัวอักษร ถาม .
งาน พลังงานภายใน และความร้อน วัดกันในหน่วยเดียวกัน - จูล ( เจ) เช่นเดียวกับพลังงานชนิดใดๆ
ในการวัดความร้อน ก่อนหน้านี้หน่วยพลังงานพิเศษถูกใช้เป็นหน่วยปริมาณความร้อน - แคลอรี่ ( อุจจาระ), เท่ากับ ปริมาณความร้อนที่ต้องทำให้น้ำ 1 กรัมร้อนขึ้น 1 องศาเซลเซียส (แม่นยำยิ่งขึ้นจาก 19.5 ถึง 20.5 ° C) โดยเฉพาะหน่วยนี้ใช้ในการคำนวณปริมาณการใช้ความร้อน (พลังงานความร้อน) ค่ะ อาคารอพาร์ตเมนต์. มีการทดลองสร้างความเทียบเท่าเชิงกลของความร้อน - ความสัมพันธ์ระหว่างแคลอรี่และจูล: 1 แคลอรี่ = 4.2 เจ.
เมื่อร่างกายถ่ายเทความร้อนจำนวนหนึ่งโดยไม่ทำงาน พลังงานภายในก็จะเพิ่มขึ้น ถ้าร่างกายปล่อยความร้อนออกมาในระดับหนึ่ง พลังงานภายในก็จะลดลง
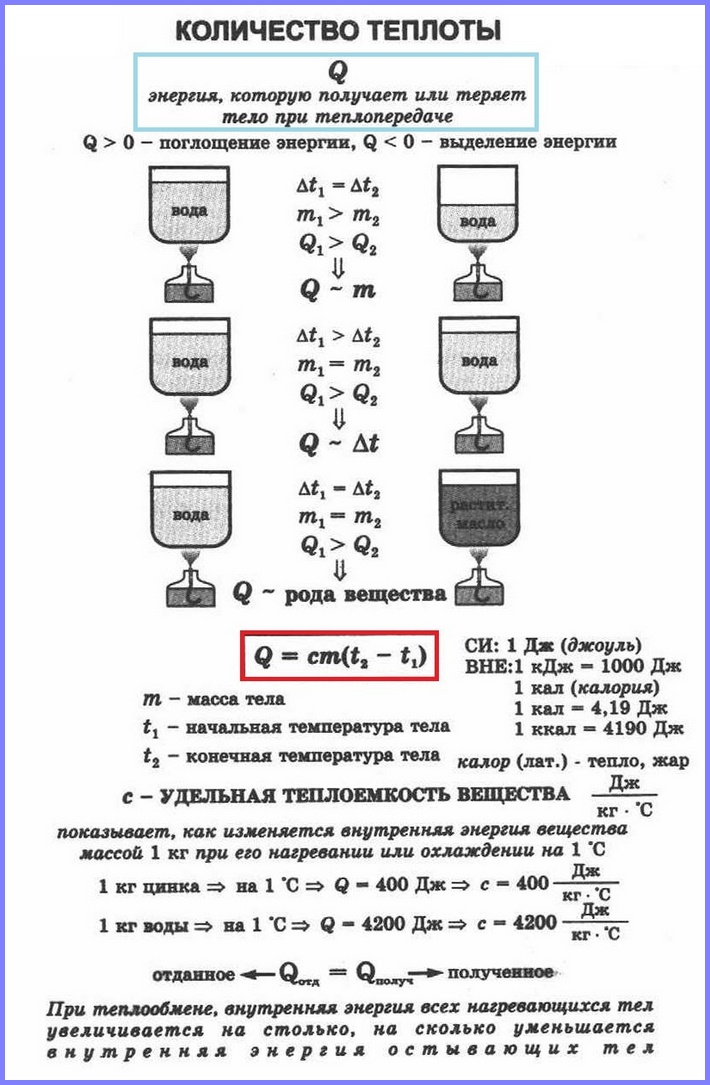
หากคุณเทน้ำ 100 กรัมลงในภาชนะที่เหมือนกันสองใบ โดยใบหนึ่งและอีกใบ 400 กรัมที่อุณหภูมิเดียวกันและวางไว้บนเตาที่เหมือนกัน น้ำในภาชนะใบแรกจะเดือดเร็วขึ้น ดังนั้น ยิ่งมวลกายมีมาก ปริมาณความร้อนที่ต้องใช้ในการวอร์มก็มากขึ้นตามไปด้วย การระบายความร้อนก็เหมือนกัน

ปริมาณความร้อนที่ต้องใช้ในการให้ความร้อนแก่ร่างกายยังขึ้นอยู่กับชนิดของสารที่ร่างกายสร้างขึ้นด้วย การขึ้นอยู่กับปริมาณความร้อนที่ต้องใช้ในการให้ความร้อนแก่ร่างกายกับประเภทของสารนี้มีลักษณะเป็นปริมาณทางกายภาพที่เรียกว่า ความจุความร้อนจำเพาะ สาร
คือปริมาณทางกายภาพเท่ากับปริมาณความร้อนที่ต้องให้สาร 1 กิโลกรัมเพื่อให้ความร้อนขึ้น 1 °C (หรือ 1 K) สาร 1 กิโลกรัมจะปล่อยความร้อนในปริมาณเท่ากันเมื่อถูกทำให้เย็นลง 1 °C
ความจุความร้อนจำเพาะถูกกำหนดโดยตัวอักษร กับ. หน่วยความจุความร้อนจำเพาะคือ 1 เจ/กก. °Cหรือ 1 J/kg °K
ความจุความร้อนจำเพาะของสารถูกกำหนดโดยการทดลอง ของเหลวมีความจุความร้อนจำเพาะสูงกว่าโลหะ น้ำมีความร้อนจำเพาะสูงสุด ส่วนทองคำมีความร้อนจำเพาะน้อยมาก
เนื่องจากปริมาณความร้อนเท่ากับการเปลี่ยนแปลงพลังงานภายในของร่างกาย จึงอาจกล่าวได้ว่าความจุความร้อนจำเพาะแสดงให้เห็นว่าพลังงานภายในเปลี่ยนแปลงไปมากเพียงใด 1 กกสารเมื่ออุณหภูมิเปลี่ยนแปลงไป 1 องศาเซลเซียส. โดยเฉพาะอย่างยิ่งพลังงานภายในของตะกั่ว 1 กิโลกรัมจะเพิ่มขึ้น 140 J เมื่อได้รับความร้อน 1 °C และลดลง 140 J เมื่อเย็นลง
ถามจำเป็นต้องให้ความร้อนแก่ร่างกายที่มีมวล มเกี่ยวกับอุณหภูมิ ที 1 °ซจนถึงอุณหภูมิ อุณหภูมิ 2 องศาเซลเซียสเท่ากับผลคูณของความจุความร้อนจำเพาะของสาร มวลกาย และความแตกต่างระหว่างอุณหภูมิสุดท้ายและอุณหภูมิเริ่มต้น กล่าวคือQ = ค ∙ ม. (เสื้อ 2 - เสื้อ 1)
สูตรเดียวกันนี้ใช้ในการคำนวณปริมาณความร้อนที่ร่างกายปล่อยออกมาเมื่อเย็นลง เฉพาะในกรณีนี้เท่านั้นที่ควรลบอุณหภูมิสุดท้ายออกจากอุณหภูมิเริ่มต้น เช่น ลบอุณหภูมิที่น้อยกว่าออกจากอุณหภูมิที่ใหญ่กว่า

นี่คือบทสรุปของหัวข้อ “ปริมาณความร้อน ความร้อนจำเพาะ". เลือกขั้นตอนถัดไป:
- ไปที่บทสรุปถัดไป:
ความจุความร้อน- คือปริมาณความร้อนที่ร่างกายดูดซึมเมื่อถูกความร้อน 1 องศา
ความจุความร้อนของร่างกายระบุด้วยอักษรละตินตัวพิมพ์ใหญ่ กับ.
ความจุความร้อนของร่างกายขึ้นอยู่กับอะไร? ก่อนอื่นจากมวลของมัน เห็นได้ชัดว่าการให้ความร้อน เช่น น้ำ 1 กิโลกรัม จะต้องใช้ความร้อนมากกว่าการให้ความร้อน 200 กรัม
แล้วชนิดของสารล่ะ? มาทำการทดลองกัน ลองเอาภาชนะที่เหมือนกันสองใบแล้วเทน้ำที่มีน้ำหนัก 400 กรัมลงในหนึ่งในนั้นและอีกใบหนึ่ง - น้ำมันพืชมีน้ำหนัก 400 กรัม มาเริ่มทำความร้อนโดยใช้หัวเผาที่เหมือนกันกันดีกว่า เมื่อสังเกตค่าเทอร์โมมิเตอร์เราจะเห็นว่าน้ำมันร้อนขึ้นอย่างรวดเร็ว หากต้องการให้น้ำร้อนและน้ำมันมีอุณหภูมิเท่ากัน จะต้องทำให้น้ำร้อนนานขึ้น แต่ยิ่งเราให้น้ำร้อนนานเท่าไรก็ยิ่งได้รับความร้อนจากเตามากขึ้นเท่านั้น
ดังนั้นปริมาณความร้อนที่แตกต่างกันจึงจำเป็นในการให้ความร้อนแก่สารต่าง ๆ ที่มีมวลเท่ากันจนถึงอุณหภูมิเดียวกัน ปริมาณความร้อนที่ต้องใช้ในการให้ความร้อนแก่ร่างกาย ดังนั้น ความจุความร้อนของมันจึงขึ้นอยู่กับชนิดของสารที่ร่างกายประกอบขึ้น
ตัวอย่างเช่น ในการเพิ่มอุณหภูมิของน้ำที่มีน้ำหนัก 1 กิโลกรัมขึ้น 1°C จำเป็นต้องมีปริมาณความร้อนเท่ากับ 4,200 จูล และเพื่อให้ความร้อนแก่มวลเดียวกันขึ้น 1°C น้ำมันดอกทานตะวันปริมาณความร้อนที่ต้องการคือ 1,700 J
ปริมาณทางกายภาพแสดงว่าต้องใช้ความร้อนเท่าใดในการทำให้สาร 1 กิโลกรัมร้อนขึ้น 1 ºСเรียกว่า ความจุความร้อนจำเพาะ ของสารนี้
สารแต่ละชนิดมีความจุความร้อนจำเพาะของตัวเอง ซึ่งแสดงด้วยตัวอักษรละติน c และมีหน่วยวัดเป็นจูลต่อกิโลกรัม (J/(kg °C))
ความจุความร้อนจำเพาะของสารชนิดเดียวกันในสถานะการรวมกลุ่มที่แตกต่างกัน (ของแข็ง ของเหลว และก๊าซ) จะแตกต่างกัน ตัวอย่างเช่น ความจุความร้อนจำเพาะของน้ำคือ 4200 J/(kg °C) และความจุความร้อนจำเพาะของน้ำแข็งคือ 2100 J/(kg °C) อลูมิเนียมในสถานะของแข็งมีความจุความร้อนจำเพาะ 920 J/(kg - °C) และในสถานะของเหลว - 1,080 J/(kg - °C)
โปรดทราบว่าน้ำมีความจุความร้อนจำเพาะสูงมาก ดังนั้นน้ำในทะเลและมหาสมุทรซึ่งร้อนขึ้นในฤดูร้อนจึงถูกดูดซับจากอากาศ จำนวนมากความร้อน. ด้วยเหตุนี้ ในสถานที่ที่อยู่ใกล้แหล่งน้ำขนาดใหญ่ ฤดูร้อนจึงไม่ร้อนเท่ากับในสถานที่ห่างไกลจากน้ำ
การคำนวณปริมาณความร้อนที่ต้องใช้ในการทำความร้อนให้กับร่างกายหรือที่ร่างกายปล่อยออกมาระหว่างการทำความเย็น
จากที่กล่าวมาข้างต้น เป็นที่ชัดเจนว่าปริมาณความร้อนที่ต้องใช้ในการให้ความร้อนแก่ร่างกายขึ้นอยู่กับชนิดของสารที่ร่างกายประกอบด้วย (เช่น ความจุความร้อนจำเพาะของสารนั้น) และมวลของร่างกาย เป็นที่ชัดเจนว่าปริมาณความร้อนขึ้นอยู่กับว่าเราจะเพิ่มอุณหภูมิของร่างกายกี่องศา
ดังนั้น เพื่อกำหนดปริมาณความร้อนที่ต้องใช้ในการทำความร้อนให้กับร่างกายหรือที่ร่างกายปล่อยออกมาในระหว่างการทำความเย็น คุณจะต้องคูณความจุความร้อนจำเพาะของร่างกายด้วยมวลของมัน และด้วยความแตกต่างระหว่างอุณหภูมิสุดท้ายและอุณหภูมิเริ่มต้น:
ถาม= ซม (เสื้อ 2 -เสื้อ 1),
ที่ไหน ถาม- ปริมาณความร้อน ค- ความจุความร้อนจำเพาะ ม- มวลร่างกาย, เสื้อ 1- อุณหภูมิเริ่มต้น เสื้อ 2- อุณหภูมิสุดท้าย
เมื่อร่างกายเกิดความร้อนขึ้น เสื้อ 2> เสื้อ 1และดังนั้นจึง ถาม >0 . เมื่อร่างกายเย็นลง ที 2 ไอ< เสื้อ 1และดังนั้นจึง ถาม< 0 .
หากทราบความจุความร้อนของร่างกายทั้งหมด กับ, ถามกำหนดโดยสูตร: ถาม = C (เสื้อ 2 - เสื้อ 1)
22) การหลอม: คำจำกัดความ, การคำนวณปริมาณความร้อนสำหรับการหลอมละลายหรือการแข็งตัว, ความร้อนจำเพาะของการหลอมเหลว, กราฟของ t 0 (Q)
อุณหพลศาสตร์
สาขาวิชาฟิสิกส์โมเลกุลที่ศึกษาการถ่ายโอนพลังงาน รูปแบบของการเปลี่ยนแปลงพลังงานประเภทหนึ่งไปเป็นอีกประเภทหนึ่ง อุณหพลศาสตร์ไม่ได้คำนึงถึงอุณหพลศาสตร์ซึ่งต่างจากทฤษฎีจลน์ศาสตร์ระดับโมเลกุล โครงสร้างภายในสารและไมโครพารามิเตอร์
ระบบอุณหพลศาสตร์
เป็นกลุ่มของวัตถุที่แลกเปลี่ยนพลังงาน (ในรูปของงานหรือความร้อน) ระหว่างกันหรือกับกัน สิ่งแวดล้อม. ตัวอย่างเช่น น้ำในกาต้มน้ำเย็นลง และมีการแลกเปลี่ยนความร้อนระหว่างน้ำกับกาต้มน้ำและความร้อนของกาต้มน้ำกับสิ่งแวดล้อม กระบอกสูบที่มีแก๊สอยู่ใต้ลูกสูบ: ลูกสูบทำงานซึ่งเป็นผลมาจากการที่ก๊าซได้รับพลังงานและพารามิเตอร์มาโครเปลี่ยนไป
ปริมาณความร้อน
นี้ พลังงานซึ่งระบบรับหรือปล่อยออกมาระหว่างกระบวนการแลกเปลี่ยนความร้อน แสดงด้วยสัญลักษณ์ Q ซึ่งวัดได้เช่นเดียวกับพลังงานใดๆ ในหน่วยจูล
จากกระบวนการแลกเปลี่ยนความร้อนต่างๆ พลังงานที่ถ่ายโอนจะถูกกำหนดด้วยวิธีของมันเอง
เครื่องทำความร้อนและความเย็น
กระบวนการนี้มีลักษณะเฉพาะคือการเปลี่ยนแปลงอุณหภูมิของระบบ ปริมาณความร้อนถูกกำหนดโดยสูตร

ความจุความร้อนจำเพาะของสารด้วยวัดจากปริมาณความร้อนที่ต้องใช้ในการอุ่นเครื่อง หน่วยมวลของสารนี้ 1K ต้องใช้แก้ว 1 กก. หรือน้ำ 1 กก. ในการทำความร้อน ปริมาณที่แตกต่างกันพลังงาน. ความจุความร้อนจำเพาะเป็นปริมาณที่ทราบ ซึ่งคำนวณไว้แล้วสำหรับสารทั้งหมด ดูค่าในตารางทางกายภาพ
ความจุความร้อนของสาร C- นี่คือปริมาณความร้อนที่จำเป็นในการทำให้ร่างกายร้อนขึ้นโดยไม่คำนึงถึงมวลของมัน 1K


การหลอมละลายและการตกผลึก
การหลอมละลายคือการเปลี่ยนสารจากของแข็งเป็นสถานะของเหลว การเปลี่ยนผ่านแบบย้อนกลับเรียกว่าการตกผลึก
พลังงานที่ใช้ในการทำลายโครงผลึกของสารจะถูกกำหนดโดยสูตร


ความร้อนจำเพาะของฟิวชันเป็นค่าที่ทราบของสารแต่ละชนิด ดูค่าในตารางทางกายภาพ
การกลายเป็นไอ (การระเหยหรือการเดือด) และการควบแน่น
การกลายเป็นไอคือการเปลี่ยนของสารจากสถานะของเหลว (ของแข็ง) ไปเป็นสถานะก๊าซ กระบวนการย้อนกลับเรียกว่าการควบแน่น


ความร้อนจำเพาะของการกลายเป็นไอเป็นค่าที่ทราบของสารแต่ละชนิด ดูค่าในตารางทางกายภาพ
การเผาไหม้
ปริมาณความร้อนที่ปล่อยออกมาเมื่อสารไหม้


ความร้อนจำเพาะของการเผาไหม้เป็นค่าที่ทราบของสารแต่ละชนิด ดูค่าในตารางทางกายภาพ
สำหรับระบบของร่างกายแบบปิดและแบบอะเดียแบติก สมการสมดุลความร้อนจะเป็นไปตามสมการ ผลรวมเชิงพีชคณิตของปริมาณความร้อนที่ให้และรับโดยทุกวัตถุที่มีส่วนร่วมในการแลกเปลี่ยนความร้อนเท่ากับศูนย์:
ค 1 +คิว 2 +...+คิว n =0
23) โครงสร้างของของเหลว ชั้นพื้นผิว แรงตึงผิว: ตัวอย่างของการสำแดง การคำนวณ ค่าสัมประสิทธิ์แรงตึงผิว
ในบางครั้ง โมเลกุลใดๆ ก็ตามอาจเคลื่อนที่ไปยังตำแหน่งว่างในบริเวณใกล้เคียง การกระโดดของของเหลวเกิดขึ้นค่อนข้างบ่อย ดังนั้นโมเลกุลจึงไม่ผูกติดกับจุดศูนย์กลางเฉพาะเหมือนในผลึก และสามารถเคลื่อนที่ได้ตลอดปริมาตรของของเหลว สิ่งนี้จะอธิบายความลื่นไหลของของเหลว เนื่องจากปฏิสัมพันธ์ที่รุนแรงระหว่างโมเลกุลที่อยู่ใกล้กัน พวกมันจึงสามารถสร้างกลุ่มที่ได้รับคำสั่งเฉพาะที่ (ไม่เสถียร) ซึ่งมีหลายโมเลกุลได้ ปรากฏการณ์นี้เรียกว่า ปิดรับออเดอร์(รูปที่ 3.5.1)
สัมประสิทธิ์ β เรียกว่า ค่าสัมประสิทธิ์อุณหภูมิของการขยายตัวเชิงปริมาตร . ค่าสัมประสิทธิ์ของของเหลวนี้มากกว่าของแข็งหลายสิบเท่า ตัวอย่างเช่น สำหรับน้ำ ที่อุณหภูมิ 20 °C β ใน พรีเมี่ยม 2 10 – 4 K – 1 สำหรับเหล็ก β st พรีเมี่ยม 3.6 10 – 5 K – 1 สำหรับแก้วควอทซ์ β kv หยาบคาย 9 10 – 6 K - 1 .
การขยายตัวทางความร้อนของน้ำทำให้เกิดความผิดปกติที่น่าสนใจและสำคัญต่อสิ่งมีชีวิตบนโลก ที่อุณหภูมิต่ำกว่า 4 °C น้ำจะขยายตัวเมื่ออุณหภูมิลดลง (β< 0). Максимум плотности ρ в = 10 3 кг/м 3 вода имеет при температуре 4 °С.
เมื่อน้ำกลายเป็นน้ำแข็ง มันจะขยายตัว น้ำแข็งจึงลอยอยู่บนผิวน้ำที่กลายเป็นน้ำแข็ง อุณหภูมิของน้ำเยือกแข็งใต้น้ำแข็งคือ 0 °C ในชั้นน้ำที่มีความหนาแน่นมากขึ้นที่ด้านล่างของอ่างเก็บน้ำ อุณหภูมิจะอยู่ที่ประมาณ 4 °C ด้วยเหตุนี้ ชีวิตจึงสามารถดำรงอยู่ในน้ำจากอ่างเก็บน้ำที่กลายเป็นน้ำแข็งได้
ที่สุด คุณสมบัติที่น่าสนใจของเหลวคือการมีอยู่ พื้นผิวฟรี . ของเหลวไม่เหมือนกับก๊าซตรงที่ไม่สามารถเติมปริมาตรทั้งหมดของภาชนะที่เทลงไปได้ ส่วนต่อประสานถูกสร้างขึ้นระหว่างของเหลวกับก๊าซ (หรือไอ) ซึ่งอยู่ในสภาพพิเศษเมื่อเปรียบเทียบกับของเหลวอื่น ๆ ควรคำนึงว่าเนื่องจากความสามารถในการอัดที่ต่ำมากจึงมีชั้นพื้นผิวที่อัดแน่นมากขึ้น ไม่นำไปสู่การเปลี่ยนแปลงปริมาตรของของเหลวที่เห็นได้ชัดเจน หากโมเลกุลเคลื่อนที่จากพื้นผิวไปสู่ของเหลว แรงอันตรกิริยาระหว่างโมเลกุลจะทำงานในเชิงบวก ในทางตรงกันข้าม เพื่อดึงโมเลกุลจำนวนหนึ่งจากความลึกของของเหลวไปยังพื้นผิว (เช่น เพิ่มพื้นที่ผิวของของเหลว) แรงภายนอกจะต้องทำงานเชิงบวก Δ กภายนอกเป็นสัดส่วนกับการเปลี่ยนแปลง Δ สพื้นที่ผิว:
เป็นที่ทราบกันดีจากกลศาสตร์ว่าสภาวะสมดุลของระบบสอดคล้องกับค่าต่ำสุดของพลังงานศักย์ ตามมาว่าพื้นผิวอิสระของของเหลวมีแนวโน้มที่จะลดพื้นที่ลง ด้วยเหตุนี้ ของเหลวที่หยดหนึ่งจึงมีรูปร่างเป็นทรงกลม ของเหลวมีพฤติกรรมราวกับว่าแรงที่กระทำต่อพื้นผิวของมันกำลังหดตัว (ดึง) พื้นผิวนี้ กองกำลังเหล่านี้เรียกว่า แรงตึงผิว .
การมีอยู่ของแรงตึงผิวทำให้พื้นผิวของของเหลวดูเหมือนฟิล์มยืดแบบยืดหยุ่น โดยมีข้อแตกต่างเพียงอย่างเดียวคือแรงยืดหยุ่นในฟิล์มขึ้นอยู่กับพื้นที่ผิวของมัน (เช่น วิธีการเปลี่ยนรูปของฟิล์ม) และแรงตึงผิว กองกำลัง ไม่ต้องพึ่งบนพื้นที่ผิวของของเหลว
ของเหลวบางชนิด เช่น น้ำสบู่ มีความสามารถในการสร้างฟิล์มบางๆ ฟองสบู่ที่รู้จักกันดีมีรูปร่างเป็นทรงกลมปกติ ซึ่งยังแสดงให้เห็นถึงผลกระทบของแรงตึงผิวด้วย หากโครงลวดซึ่งด้านใดด้านหนึ่งสามารถเคลื่อนย้ายได้ถูกหย่อนลงในสารละลายสบู่ทั้งเฟรมจะถูกคลุมด้วยฟิล์มของเหลว (รูปที่ 3.5.3)
แรงตึงผิวมีแนวโน้มที่จะลดพื้นผิวของฟิล์ม เพื่อให้สมดุลด้านที่เคลื่อนย้ายได้ของเฟรมจะต้องใช้แรงภายนอกเข้าที่ หากคานประตูเคลื่อนที่ตาม Δ ภายใต้อิทธิพลของแรง xจากนั้นงาน Δ จะถูกดำเนินการ กวน์ = เอฟ vn Δ x = Δ อีพี = σΔ สโดยที่ ∆ ส = 2ลΔ x– เพิ่มพื้นที่ผิวทั้งสองด้านของฟิล์มสบู่ เนื่องจากโมดูลัสของแรงและเหมือนกัน เราสามารถเขียนได้:
|
ดังนั้น ค่าสัมประสิทธิ์แรงตึงผิว σ สามารถนิยามได้เป็น โมดูลัสของแรงตึงผิวที่กระทำต่อความยาวหน่วยของเส้นที่ล้อมรอบพื้นผิว.
เนื่องจากการกระทำของแรงตึงผิวในหยดของเหลวและภายใน ฟองสบู่แรงดันส่วนเกิน Δ เกิดขึ้น พี. หากคุณตัดรัศมีหยดทรงกลมทางจิตใจ รออกเป็นสองซีก จากนั้นแต่ละซีกจะต้องอยู่ในสมดุลภายใต้การกระทำของแรงตึงผิวที่ใช้กับขอบเขตการตัดที่มีความยาว 2π รและแรงกดดันส่วนเกินที่กระทำต่อพื้นที่ π ร 2 ส่วน (รูปที่ 3.5.4) สภาวะสมดุลเขียนเป็น
หากแรงเหล่านี้มากกว่าแรงปฏิสัมพันธ์ระหว่างโมเลกุลของของเหลวเองแสดงว่าเป็นของเหลว เปียกพื้นผิว แข็ง. ในกรณีนี้ ของเหลวเข้าใกล้พื้นผิวของของแข็งด้วยมุมแหลมที่แน่นอน θ ซึ่งเป็นลักษณะของคู่ของเหลว-ของแข็งที่กำหนด มุม θ เรียกว่า มุมสัมผัส . หากแรงปฏิกิริยาระหว่างโมเลกุลของเหลวเกินแรงปฏิกิริยากับโมเลกุลของแข็ง มุมสัมผัส θ จะกลายเป็นมุมป้าน (รูปที่ 3.5.5) ในกรณีนี้เค้าบอกว่าเป็นของเหลว ไม่เปียกพื้นผิวของของแข็ง ที่ ทำให้เปียกอย่างสมบูรณ์θ = 0, ณ ไม่เปียกอย่างสมบูรณ์θ = 180°
ปรากฏการณ์ของเส้นเลือดฝอยเรียกว่าการขึ้นหรือลงของของเหลวในท่อขนาดเส้นผ่านศูนย์กลางเล็ก - เส้นเลือดฝอย. ของเหลวที่เปียกจะลอยขึ้นผ่านเส้นเลือดฝอย ของเหลวที่ไม่เปียกจะไหลลงมา
ในรูป 3.5.6 แสดงท่อคาปิลลารีในรัศมีที่กำหนด รลดลงที่ปลายล่างเป็นของเหลวเปียกที่มีความหนาแน่น ρ ปลายด้านบนของเส้นเลือดฝอยเปิดอยู่ การเพิ่มขึ้นของของเหลวในเส้นเลือดฝอยจะดำเนินต่อไปจนกระทั่งแรงโน้มถ่วงที่กระทำต่อคอลัมน์ของของเหลวในเส้นเลือดฝอยจะมีขนาดเท่ากันกับผลลัพธ์ เอฟแรงตึงผิวที่กระทำตามแนวขอบเขตการสัมผัสของของเหลวกับพื้นผิวของเส้นเลือดฝอย: เอฟเสื้อ = เอฟที่ไหน เอฟเสื้อ = มก = ρ ชม.π ร 2 ก, เอฟ n = σ2π รเพราะ θ
นี่หมายถึง:
เมื่อทำให้ไม่เปียกโดยสมบูรณ์ θ = 180°, cos θ = –1 และด้วยเหตุนี้ ชม. < 0. Уровень несмачивающей жидкости в капилляре опускается ниже уровня жидкости в сосуде, в которую опущен капилляр.
น้ำทำให้พื้นผิวกระจกที่สะอาดเปียกจนเกือบหมด ในทางตรงกันข้าม สารปรอทไม่ได้ทำให้พื้นผิวกระจกเปียกจนหมด ดังนั้นระดับปรอทในเส้นเลือดฝอยแก้วจึงลดลงต่ำกว่าระดับในภาชนะ
24) การกลายเป็นไอ: คำจำกัดความ, ประเภท (การระเหย, การเดือด), การคำนวณปริมาณความร้อนสำหรับการกลายเป็นไอและการควบแน่น, ความร้อนจำเพาะของการกลายเป็นไอ
การระเหยและการควบแน่น คำอธิบายปรากฏการณ์การระเหยตามแนวคิดเกี่ยวกับโครงสร้างโมเลกุลของสสาร ความร้อนจำเพาะของการกลายเป็นไอ หน่วยของมัน.
เรียกว่าปรากฏการณ์การเปลี่ยนของเหลวให้เป็นไอ การกลายเป็นไอ
การระเหย - กระบวนการกลายเป็นไอที่เกิดขึ้นจากพื้นผิวเปิด
โมเลกุลของของเหลวเคลื่อนที่ด้วยความเร็วที่ต่างกัน หากโมเลกุลใดมาจบลงที่พื้นผิวของของเหลว ก็สามารถเอาชนะแรงดึงดูดของโมเลกุลข้างเคียงและลอยออกจากของเหลวได้ โมเลกุลที่ถูกพ่นออกมาจะเกิดไอน้ำ โมเลกุลที่เหลือของของเหลวจะเปลี่ยนความเร็วเมื่อชนกัน ในเวลาเดียวกัน โมเลกุลบางตัวมีความเร็วเพียงพอที่จะบินออกจากของเหลวได้ กระบวนการนี้ดำเนินต่อไปเพื่อให้ของเหลวระเหยช้าๆ
*อัตราการระเหยขึ้นอยู่กับชนิดของของเหลว ของเหลวที่มีโมเลกุลถูกดึงดูดด้วยแรงน้อยกว่าจะระเหยเร็วขึ้น
*การระเหยสามารถเกิดขึ้นได้ที่อุณหภูมิใดก็ได้ แต่เมื่อ อุณหภูมิสูงการระเหยจะเกิดขึ้นเร็วขึ้น .
*อัตราการระเหยขึ้นอยู่กับพื้นที่ผิว
*เมื่อมีลม (การไหลของอากาศ) การระเหยจะเกิดขึ้นเร็วขึ้น
ในระหว่างการระเหยพลังงานภายในจะลดลงเนื่องจาก ในระหว่างการระเหย ของเหลวจะออกจากโมเลกุลที่รวดเร็ว ดังนั้น ความเร็วเฉลี่ยโมเลกุลที่เหลือจะลดลง ซึ่งหมายความว่าหากไม่มีพลังงานไหลเข้ามาจากภายนอก อุณหภูมิของของเหลวก็จะลดลง
 ปรากฏการณ์ไอระเหยกลายเป็นของเหลว เรียกว่า การควบแน่น
มันมาพร้อมกับการปลดปล่อยพลังงาน
ปรากฏการณ์ไอระเหยกลายเป็นของเหลว เรียกว่า การควบแน่น
มันมาพร้อมกับการปลดปล่อยพลังงาน
การควบแน่นของไอน้ำอธิบายการก่อตัวของเมฆ ไอน้ำที่ลอยขึ้นมาเหนือพื้นดินก่อตัวเป็นเมฆในชั้นอากาศเย็นตอนบน ซึ่งประกอบด้วยหยดน้ำเล็กๆ
ความร้อนจำเพาะของการกลายเป็นไอ - ทางกายภาพ ค่าที่แสดงปริมาณความร้อนที่จำเป็นในการเปลี่ยนของเหลวน้ำหนัก 1 กิโลกรัมให้เป็นไอน้ำโดยไม่เปลี่ยนอุณหภูมิ
อุดร ความร้อนของการกลายเป็นไอ แสดงด้วยตัวอักษร L และวัดเป็น J/kg
อุดร ความร้อนของการระเหยของน้ำ: L=2.3×10 6 J/kg, แอลกอฮอล์ L=0.9×10 6
ปริมาณความร้อนที่ต้องใช้ในการเปลี่ยนของเหลวให้เป็นไอ: Q = Lm


